
2023年以來,港股市場走勢疲軟,生物科技板塊持續承壓,大批醫藥企業都遭遇了股價的持續下跌,科濟藥業-B(02171.HK)亦是如此。
12月13日,該股再度遭遇跳空放量暴跌,截至收盤,其股價跌幅達到30.4%,創下了上市以來的新低,資金出逃迹象也比較明顯。

從近期的情況來看,該公司似乎遇到了一些「麻煩」。
三款候選藥物被FDA叫停臨床試驗
科濟藥業是一家在中國及美國擁有業務的生物制藥公司,主要專注於治療實體瘤和血液惡性腫瘤的創新嵌合抗原受體T細胞(CAR-T)療法。
從研發管線來看,該公司的主要候選產品澤沃基奧侖賽注射液(研發代號:CT053),是一種用於治療復發/難治多發性骨髓瘤的自體BCMA CAR-T細胞候選產品,在管線中最接近商業化。
此外,科濟藥業的實體瘤候選產品CT041處於確證性II期臨床試驗、CT011處於I期臨床試驗,AB011處於Ib期臨床試驗階段。

CAR-T療法是一種治療腫瘤的新型精準靶向療法。這種定制化療法在收集患者體内T細胞後,在體外利用基因工程手段將T細胞改造成CAR-T細胞,經體外擴增培養後回輸到患者體内進行治療腫瘤的方法,有著「抗癌神藥」之稱,尤其被視為是改變血液癌症治療的革命性方法,因而受到廣泛關注。
而科濟藥業股價大跌就是因為旗下三款CAR-T療法候選產品出了一些狀況。
12月12日盤後,科濟藥業發佈公告稱,公司在美國的子公司收到美國食品藥品監督管理局(「FDA」)的通知,要求暫停CT053、CT041和CT071的臨床試驗,等待對位於北卡羅來納州達勒姆的生產基地進行檢查後得出的結論。
這則公告引發了投資者的擔憂。
不過,科濟藥業稱,FDA並未針對公司臨床數據提出疑問,此次FDA的專業建議主要是因CMC(化學、制造和控制)相關問題,有些員工培訓等遺留問題需進行合規完善,並非針對工藝問題。
科濟藥業亦在公告中表示,公司將對現行藥品生產質量管理規範(cGMP)進行全面檢查和改進,並承諾與FDA密切合作,解決檢查發現的問題,以確保臨床試驗和上市申請的順利進行和高質量生產。
CAR-T療法遭遇調查,科濟藥業早已「受創」
雖然科濟藥業在儘力解釋,但從股價的走勢及成交量來看,市場資金顯然並不買賬。
之所以市場資金的信心如此不足,或許還是受到了日前另一則消息的影響。
11月28日(當地時間),FDA官網發佈公告稱,目前獲得批準的所有靶向BCMA和CD19的CAR-T療法存在引發T細胞惡性腫瘤(包括嵌合抗原受體CAR陽性淋巴瘤)的風險。
FDA還表示,儘管這些產品在獲批適應症治療中帶來的總體健康獲益仍大於其潛在風險,但該機構仍在調查這些產品帶來的T細胞惡性腫瘤風險,包括住院治療和死亡病例,並正在評估採取監管行動的必要性。
據悉,美股市場的諾華制藥(NVS.US)、百時美施貴寶(BMY.US)、吉利德科學(GILD.US)等公司旗下擁有CAR-T療法相關產品。
而國内目前獲批上市的CAR-T療法產品共4個,涉及藥明巨諾等公司。
在FDA公佈上述消息後,美國相關企業也進行了回應。
其中,百時美施貴寶表示,在使用過公司CAR-T產品Abecma治療的4700名患者中,沒有一例出現T細胞惡性腫瘤。諾華制藥、吉利德科學也稱,在目前接受治療的患者中,未發現其與新發惡性腫瘤的發展有因果關系。
此外,國内藥企亦有回應。藥明巨諾表示,有留意到FDA的信息,公司的倍諾達(瑞基奧侖賽注射液)治療了幾百名患者,暫時並未發現類似的風險。
而科濟藥業則回應稱,截至目前,在研CAR-T產品,臨床試驗治療患者總數超過500例,靶向BCMA CAR-T產品達250餘例,未觀察到T細胞淋巴瘤案例。此次事件對公司產品的研發和商業化進程沒有實質影響。
值得一提的是,從二級市場的反應來看,擁有商業化CAR-T相關產品的上市企業受到的影響要小得多,而擁有在研CAR-T產品的上市公司的股價受到的影響顯然更重。
其中,科濟藥業受影響比較大,其股價在11月29日就遭遇放量大跌23.29%。
雖然在出現「利空」消息之後,科濟藥業均進行了積極回應,但效果顯然不大好,如今CT053、CT041和CT071三款候選產品被FDA叫停臨床試驗很難不讓投資者聯想到這是FDA採取的進一步的監管行動,投資者的信心更加不足了。
業績持續虧損,CT053被寄予厚望
這背後的邏輯在於,科濟藥業還在持續虧損,而此次被叫停臨床試驗的澤沃基奧侖賽注射液(研發代號:CT053)、CT041被寄予厚望,海外對這款產品來說又非常重要,因此一點風吹草動就容易引發投資者的避險出逃。
數據顯示,因為沒有商業化產品,該公司在2021年以外的其餘年份均沒有錄得任何的收入。而各項費用一直在支出,科濟藥業一直處於虧損狀態。
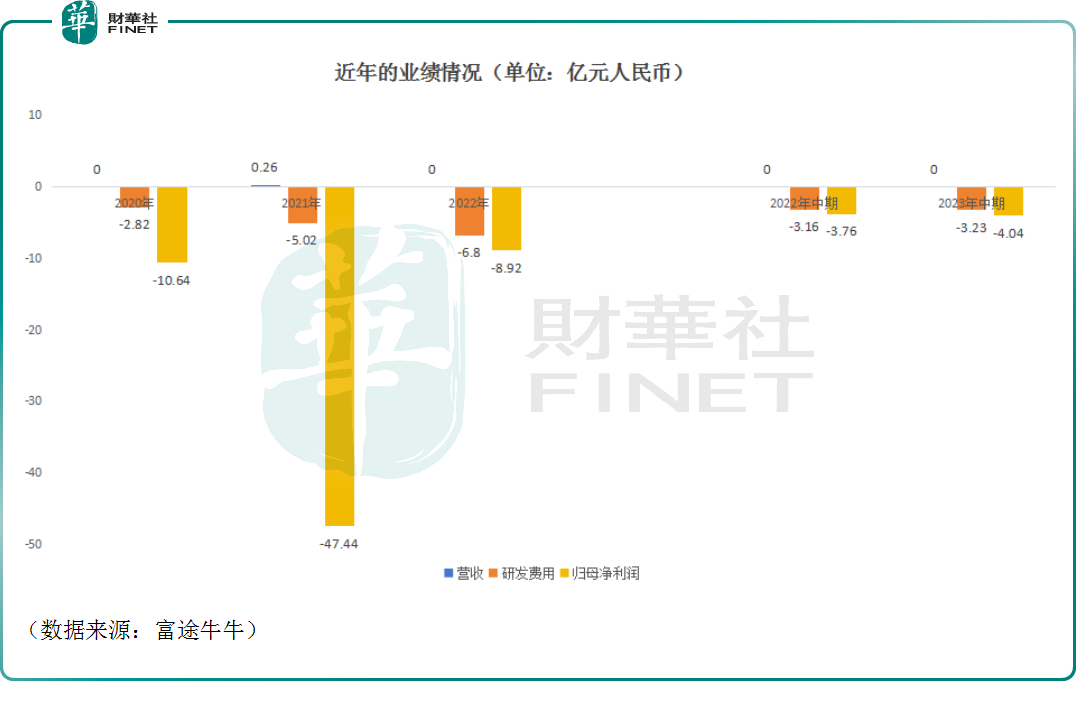
2023年上半年,科濟藥業錄得歸母淨虧損4.04億元(人民幣,下同),主要因研發開支增加及匯率變動帶來的虧損。
雖然截至2023年中期末,該公司的現金及現金等價物以及原到期日3個月至12個月的定期存款有21.74億元,不算「太窮」,但現在港股市場流動性不佳,靠二級市場籌集資金難度不小,如果科濟藥業不能實現「造血能力」的突破,賬上的錢又能燒多久?
需要指出的是,CAR-T產品除了有「抗癌神藥」之稱外,還有「天價藥」、「一針一套房」等標簽,原因在於這種藥的價格特别貴。
海外尤其是發達國家是各家藥企非常重視的一塊市場,科濟藥業亦有「出海」打算。
結合研發管線來看,2023年中報披露,澤沃基奧侖賽注射液(CT053)在美國及加拿大進行的2期臨床試驗的入組正在進行中。
此外,CT041是世界上第一款進入II期臨床試驗的治療實體瘤的CAR-T細胞候選藥物,在科濟藥業的產品管線中研發進展也處於第一梯隊。
此次這兩款藥物的臨床試驗被FDA叫停會影響科濟藥業的「出海」大計,但影響究竟有多大目前還猶未可知。
好消息在於,國内市場目前並沒有什麽動靜,科濟藥業在國内的商業化還在持續推進。
2023年中報披露,於2022年10月,中國國家藥品監督管理局已受理澤沃基奧侖賽注射液的新藥上市申請(NDA),並將該申請納入優先審評。
另外,在今年1月份,科濟藥業已經和華東醫藥(000963.SZ)全資子公司華東醫藥(杭州)有限公司關於在中國内地商業化澤沃基奧侖賽注射液簽訂合作協議,以推動澤沃基奧侖賽注射液在中國獲批及商業化。
科濟藥業在2023年中報中披露,預期澤沃基奧侖賽注射液將於2023年底或2024年初獲國家藥品監督管理局批準用於治療R/R MM(多發性骨髓瘤)。
一旦澤沃基奧侖賽注射液實現商業化上市,將有望助力科濟藥業的業績走向增長。
結語
從目前的情況來看,雖然各家藥企均稱,未發現CAR-T藥物與新發惡性腫瘤的發展有因果關系,但FDA對於CAR-T藥物的調查依然是懸在一眾藥企頭上的「達摩克利斯之劍」,對於科濟藥業的投資者來說亦是如此,後續的調查進展值得關注。
財華網所刊載內容之知識產權為財華網及相關權利人專屬所有或持有。未經許可,禁止進行轉載、摘編、複製及建立鏡像等任何使用。
如有意願轉載,請發郵件至content@finet.com.hk,獲得書面確認及授權後,方可轉載。
更多精彩內容,請登陸
財華香港網 (https://www.finethk.com/)
財華智庫網(https://www.finet.com.cn)
現代電視 (https://www.fintv.hk)